La Química Nuclear se dedica a los cambios naturales y artificiales en los núcleos de los átomos y a las reacciones químicas de las sustancias radiactivas. La radiactividad natural es el ejemplo mas conocido de la química nuclear. Dentro de esta se consideran los efectos de las emisiones radiactivas (alfa, beta, y gamma) sobre las sustancias, incluyendo a los seres vivos .
El uso cada día mas generalizado de los reactores nucleares para la producción de electricidad hace de la química nuclear una ciencia importante para todo ciudadano.
TIPOS DE EMISIONES
Los núcleos atómicos de una sustancia radiactiva no son estables y se transmutan espontáneamente en otros núcleos emitiendo partículas alfa, beta y gamma.
Las partículas alfa son átomos de He doblemente ionizados, es decir, que han perdido sus dos electrones. Por tanto, tienen dos neutrones y dos protones. Es la radiación característica de isótopos de número atómico elevado, tales como los del uranio, torio, radio, plutonio. Dada la elevada masa de estas partículas y a que se emiten a gran velocidad por los núcleos (su velocidad es del orden de 107m/s), al chocar con la materia pierden gradualmente su energía ionizando los átomos y se frenan muy rápidamente, por lo que quedan detenidas con tan sólo unos cm de aire o unas milésimas de mm de agua. En su interacción con el cuerpo humano no son capaces de atravesar la piel. Así pues, tienen poco poder de penetración siendo absorbidos totalmente por una lámina de aluminio de 0.1 mm de espesor o una simple hoja de papel.
Las partículas beta son electrones emitidos a grandes velocidades próximas a la de la luz. Debido a la menor masa que la radiación alfa, tienen más poder de penetración que las partículas alfa siendo absorbidas por una lámina de aluminio de 0.5 mm de espesor y quedan frenadas en algunos m de aire, o por 1 cm de agua. En el cuerpo humano, pueden llegar a traspasar la piel, pero no sobrepasan el tejido subcutáneo. Los positrones son partículas con masa despreciable y carga equivalente a la de un protón.
Las partículas gamma son radiaciones electromagnéticas de la misma naturaleza que los rayos X pero de menor longitud de onda. Su poder de penetración es muy elevado frente al de las partículas alfa o beta, pudiendo atravesar el cuerpo humano. Quedan frenadas con espesores de 1 m de hormigón o unos pocos cm de plomo, por lo que cuando se utilizan fuentes radiactivas que emiten este tipo de radiación, hay que utilizar blindajes adecuados.
REACCIONES NUCLEARES
Una reacción nuclear implica cambios de los átomos de uno o dos elementos en uno o mas átomos de otro u otros elementos.
E = m c2
Mediante técnicas muy precisas es posible determinar la masa de un núcleo atómico formado por una cantidad de neutrones ( que llamamos N) y otra cantidad de protones (que llamamos Z), es decir en total por A nucleones (A=N+Z). También se pueden medir la masa de un protón aislado y la de un neutrón aislado. La sorpresa es que la masa del núcleo resulta siempre menor que la suma de las masas de los nucleones que lo constituyen.
Esto parece muy raro. En la vida cotidiana esto sería equivalente por ejemplo a mezclar un kilo de harina con medio kilo de manteca y que la pasta resultante pesara menos que un kilo y medio.
La masa que falta en los núcleos atómicos cuando los formamos juntando todos los nucleones no ha desaparecido, sino que se ha transformado en energía, como lo establece la famosa relación de Einstein " E = mc2 ". Einstein dice, ¡y tiene razón!, que la energía de un cuerpo (E) es igual a su masa (m) multiplicada por la velocidad de la luz (c) al cuadrado. Cuando desaparece una cantidad de masa, aparece una cantidad equivalente de energía. En nuestra desaparición de masa al formar el núcleo, la energía que aparece es llamada energía de unión. Esa energía de unión actúa como un pegamento que une a los nucleones. Si quisiéramos separar (disociar) de vuelta todos los nucleones tendríamos que hacer fuerza a medida que los separamos, es decir tendríamos que hacer trabajo. El trabajo total que haríamos en ese caso sería igual a la energía de unión.
La energía de unión por nucleón, es decir la energía de unión dividida por el número de nucleones (A), nos indica cuánta masa perdió en promedio cada nucleón presente en el núcleo, y nos da idea de cuán "pegados" están los nucleones entre sí. Cuanto más grande es la energía de unión por nucleón, más agarrados están unos a otros y más difícil es separarlos.
No sabemos por qué esto es así, pero sabemos que la energía de unión por nucleón no es igual para todos los elementos: es pequeña para núcleos livianos (cerca del hidrógeno), se hace máxima para núcleos intermedios (cerca del hierro) y se vuelve a achicar para núcleos pesados (plomo, uranio). Esto indica que los núcleos más difíciles de disociar son justamente los núcleos medios, ya que su pérdida de masa por nucleón es la más grande.
Toda transformación de núcleos que conduzca a la formación de núcleos intermedios producirá entonces energía. Por ejemplo, si lográramos partir un núcleo de plomo en dos, los dos núcleos resultantes serían intermedios y en el proceso se liberaría energía. Si lográramos juntar dos núcleos de azufre (livianos), también formaríamos un núcleo intermedio y también obtendríamos energía. En cambio deberíamos gastar mucha energía en producir azufre partiendo un núcleo intermedio o en producir plomo juntando dos núcleos intermedios.
Estas transformaciones que pueden ocurrir en los núcleos de los átomos, y que consisten fundamentalmente en juntar o separar nucleones y/o grupos de nucleones se denominan reacciones nucleares. La energía liberada en las reacciones nucleares es la energía nuclear.
A lo largo de millones y millones de siglos las reacciones nucleares se van produciendo naturalmente en el universo. A medida que se van formando núcleos intermedios es muy difícil que ellos se destruyan por otras reacciones nucleares, ya que es más fácil que ocurra una reacción que produzca energía que otra que necesite energía (como es más fácil bajar una escalera que subirla). Esto explica por qué las estrellas más viejas tienen mucho hierro.
METODOS PARA DETECTAR RADIACIÓN
Puesto que las emisiones de las sustancias radiactivas son invisibles, se han desarrollado diversos métodos indirectos para detectarlas. Se describirán cuatro de esos métodos. Todos ellos se basan en el hecho que en los átomos y moléculas afectadas por las radiaciones, ciertos electrones se desplazan a niveles energéticos mas altos.
Métodos Fotográficos: El papel y la película fotográfica se han usado durante mucho tiempo en la detección de la radiactividad. Las emisiones afectan a la emulsión fotográfica de la misma manera que la luz visible. Despues de la exposición, el papel o película se revelan en la forma usual.
Método Fluorescente: Muchas sustancias son capaces de absorber energía radiante de longitud de onda corta (por ejemplo, rayos gamma, X, y ultravioleta) o energía cinética departiculas de alta velocidad (alfa y beta) y transformarlas en energía radiante de una longitud de onda que esta situada en la región visible por el ojo humano.
Cámaras de Niebla: Inventada en 1911 por el físico ingles C.T.R. Wilson, permite ver la trayectoria de una radiación ionizante en su paso atravez de un gas. Wilson produjo niebla artificial en el laboratorio saturando u cierto volumen de aire con vapor de agua y causando el enfriamiento de la humedad por medio de una rápida expansión . Si no están presentes iones, u otra partículas que sirvan como núcleos para condensar la niebla, el aire quedara sobre saturado de humedad. Wilson encontró que al colocar una sustancia radiactiva en el aire sobresaturado de una camara de niebla, de dicha sustancia emanaban líneas delgadas de niebla.
Contadores de ionización de gases: En un contador de ionización de gases una partícula ionizante pasa atravez de un gas entre dos electrodos cargados. Los iones formados en el gas son atraídos por los electrodos y producen pulsaciones en forma de un flojo de corriente.
USOS DE ISÓTOPOS RADIACTIVOS
La primera utilización de los isótopos radiactivos con fines experimentales se realizó en Austria en 1913, justamente diez años despues de la concesión del Premio Nobel a Henry Becquerel y Marie Curie por el descubrimiento de la Radiactividad. Fue concretamente el físico George Charles de Hevery quien utilizó un isótopo de plomo (Pb-210) para estudiar la solubilidad del sulfato y cromato de plomo.
Con el invento del ciclotrón a principios de la década de los treinta y el posterior desarrollo de los reactores nucleares en la década de los cincuenta comienza la fabricación industrial de isótopos radiactivos.
Las aplicaciones de los isótopos radiactivos son múltiples y abarcan distintos campos como la industria, medicina e investigación.
En cualquiera de estos campos se utilizan los isótopos para múltiples funciones tales como: Medida de caudales, prospecciones mineras, control de contaminación de aguas, elaboración de radiofármacos, estudios y análisis citológicos, investigación bioquímica, radiodiagnosis, tratamiento del cáncer, y otros muchos usos.
Todas estas aplicaciones son muy beneficiosas para la humanidad, pero como cualquier otra actividad genera residuos que es necesario tratar y gestionar para preservar al hombre y al medio ambiente de las acciones perniciosas de las radiaciones.
Gracias al uso de reactores nucleares hoy, en día es posible obtener importantes cantidades de material radiactivo a bajo costo. Es así como desde finales de los años 40, se produce una expansión en el empleo pacífico de diversos tipos de Isótopos Radiactivos en diversas áreas del quehacer científico y productivo del hombre.
Estas áreas se pueden clasificar en:
Agricultura y Alimentación
a)Control de Plagas.
Se sabe que algunos insectos pueden ser muy perjudiciales tanto para la calidad y productividad de cierto tipo de cosechas, como para la salud humana. En muchas regiones del planeta aún se les combate con la ayuda de gran variedad de productos químicos, muchos de ellos cuestionados o prohibidos por los efectos nocivos que producen en el organismo humano. Sin embargo, con la tecnología nuclear es posible aplicar la llamada "Técnica de los Insectos Estériles (TIE)", que consiste en suministrar altas emisiones de radiación ionizante a un cierto grupo de insectos machos mantenidos en laboratorio. Luego los machos estériles se dejan en libertad para facilitar su apareamiento con los insectos hembra. No se produce, por ende, la necesaria descendencia. De este modo, luego de sucesivas y rigurosas repeticiones del proceso, es posible controlar y disminuir su población en una determinada región geográfica. En Chile, se ha aplicado con éxito la técnica TIE para el control de la mosca de la fruta, lo que ha permitido la expansión de sus exportaciones agrícolas.
b)Mutaciones.
La irradiación aplicada a semillas, después de importantes y rigurosos estudios, permite cambiar la información genética de ciertas variedades de plantas y vegetales de consumo humano. El objetivo de la técnica, es la obtención de nuevas variedades de especies con características particulares que permitan el aumento de su resistencia y productividad.
c)Conservación de Alimentos.
En el mundo mueren cada año miles de personas como producto del hambre, por lo tanto, cada vez existe mayor preocupación por procurar un adecuado almacenamiento y mantención de los alimentos. Las radiaciones son utilizadas en muchos países para aumentar el período de conservación de muchos alimentos. Es importante señalar, que la técnica de irradiación no genera efectos secundarios en la salud humana, siendo capaz de reducir en forma considerable el número de organismos y microorganismos patógenos presentes en variados alimentos de consumo masivo.
La irradiación de alimentos es aplicada en Chile en una planta de irradiación multipropósito ubicada en el Centro de Estudios Nucleares Lo Aguirre, con una demanda que obliga a su funcionamiento ininterrumpido durante los 365 días del año.
Hidrología
Gracias al uso de las técnicas nucleares es posible desarrollar diversos estudios relacionados con recursos hídricos. En estudios de aguas superficiales es posible caracterizar y medir las corrientes de aguas lluvias y de nieve; caudales de ríos, fugas en embalses, lagos y canales y la dinámica de lagos y depósitos.
En estudios de aguas subterráneas es posible medir los caudales de las napas, identificar el origen de las aguas subterráneas, su edad, velocidad, dirección, flujo, relación con aguas superficiales, conexiones entre acuíferos, porosidad y dispersión de acuíferos.
Medicina
a)Vacunas.
Se han elaborado radiovacunas para combatir enfermedades parasitarias del ganado y que afectan la producción pecuaria en general. Los animales sometidos al tratamiento soportan durante un período más prolongado el peligro de reinfección siempre latente en su medio natural.
b)Medicina Nuclear.
Se ha extendido con gran rapidez el uso de radiaciones y de radioisótopos en medicina como agentes terapéuticos y de diagnóstico.
En el diagnóstico se utilizan radiofármacos para diversos estudios de:
- Tiroides.
- Hígado.
- Riñón.
- Metabolismo.
- Circulación sanguínea.
- Corazón.
- Pulmón.
- Trato gastrointestinales.
c)Radioinmunoanálisis.
Se trata de un método y procedimiento de gran sensibilidad utilizado para realizar mediciones de hormonas, enzimas, virus de la hepatitis, ciertas proteínas del suero, fármacos y variadas sustancias.
El procedimiento consiste en tomar muestras de sangre del paciente, donde con posterioridad se añadirá algún radioisótopo específico, el cual permite obtener mediciones de gran precisión respecto de hormonas y otras sustancias de interés.
d)Radiofármacos.
Se administra al paciente un cierto tipo de fármaco radiactivo que permite estudiar, mediante imágenes bidimensionales (centelleografía) o tridimensionales (tomografía), el estado de diversos órganos del cuerpo humano.
De este modo se puede examinar el funcionamiento de la tiroides, el pulmón, el hígado y el riñón, así como el volumen y circulación sanguíneos. También, se utilizan radiofármacos como el Cromo - 51 para la exploración del bazo, el Selenio - 75 para el estudio del páncreas y el Cobalto - 57 para el diagnóstico de la anemia.
Medio Ambiente
En esta área se utilizan técnicas nucleares para la detección y análisis de diversos contaminantes del medio ambiente. La técnica más conocida recibe el nombre de Análisis por Activación Neutrónica, basado en los trabajos desarrollados en 1936 por el científico húngaro J.G. Hevesy, Premio Nobel de Química en 1944. La técnica consiste en irradiar una muestra, de tal forma, de obtener a posteriori los espectros gamma que ella emite, para finalmente procesar la información con ayuda computacional. La información espectral identifica los elementos presentes en la muestra y las concentraciones de los mismos.
Una serie de estudios se han podido aplicar a diversos problemas de contaminación como las causadas por el bióxido de azufre, las descargas gaseosas a nivel del suelo, en derrames de petróleo, en desechos agrícolas, en contaminación de aguas y en el smog generado por las ciudades.
Industria e Investigación
a)Trazadores.
Se elaboran sustancias radiactivas que son introducidas en un determinado proceso. Luego se detecta la trayectoria de la sustancia gracias a su emisión radiactiva, lo que permite investigar diversas variables propias del proceso. Entre otras variables, se puede determinar caudales de fluidos, filtraciones, velocidades en tuberías, dinámica del transporte de materiales, cambios de fase de líquido a gas, velocidad de desgaste de materiales, etc..
b)Instrumentación.
Son instrumentos radioisótopicos que permiten realizar mediciones sin contacto físico directo. Se utilizan indicadores de nivel, de espesor o bien de densidad.
c)Imágenes.
Es posible obtener imágenes de piezas con su estructura interna utilizando radiografías en base a rayos gamma o bien con un flujo de neutrones. Estas imágenes reciben el nombre de Gammagrafía y Neutrografía respectivamente, y son de gran utilidad en la industria como método no destructivo de control de calidad. Con estos métodos se puede comprobar la calidad en soldaduras estructurales, en piezas metálicas fundidas, en piezas cerámicas, para análisis de humedad en materiales de construcción, etc..
d)Datación.
Se emplean técnicas isotópicas para determinar la edad en formaciones geológicas y arqueológicas. Una de las técnicas utiliza el Carbono-14, que consiste en determinar la cantidad de dicho isótopo contenida en un cuerpo orgánico. La radiactividad existente, debida a la presencia de Carbono-14, disminuye a la mitad cada 5730 años, por lo tanto, al medir con precisión su actividad se puede inferir la edad de la muestra.
e)Investigación.
Utilizando haces de neutrones generados por reactores, es posible llevar a cabo diversas investigaciones en el campo de las ciencias de los materiales. Por ejemplo, se puede obtener información respecto de estructuras cristalinas, defectos en sólidos, estudios de monocristales, distribuciones y concentraciones de elementos livianos en función de la profundidad en sólidos, etc..
En el ámbito de la biología, la introducción de compuestos radiactivos marcados ha permitido observar las actividades biológicas hasta en sus más mínimos detalles, dando un gran impulso a los trabajos de carácter genético.
COMENTARIOS
Dentro de la gran cantidad de usos que se le pueden da a la radiactividad, creo que es una forma correcta el usarlos para beneficio y ayuda de la humanidad, ya que es de todos bien sabido el hecho de que con estos elementos o reacciones también se pueden crear artefactos en perjuicio de la humanidad misma.
Esta clase de elementos tiene (aparte de lo ya mencionado) una infinita gama de usos, tanto en beneficio como en prejuicio humano.







![r = k[A]^{m}[B]^{n} \,\!](http://upload.wikimedia.org/math/d/7/2/d721257f573e003e652dfc0695d96a1f.png) Los términos entre corchetes son las molaridades de los reactivos y los exponentes m y n son coeficientes que, salvo en el caso de una etapa elemental no tienen por que estar relacionados con el
Los términos entre corchetes son las molaridades de los reactivos y los exponentes m y n son coeficientes que, salvo en el caso de una etapa elemental no tienen por que estar relacionados con el 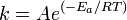

![(Foto: U. Minnesota) [Img #2185]](http://noticiasdelaciencia.com/upload/img/periodico/img_2185.jpg)
![La capucha y la máscara desarrolladas. (Foto: Mark Vorreuter) [Img #2315]](http://noticiasdelaciencia.com/upload/img/periodico/img_2315.jpg)
![(Foto: Marco Crocoli) [Img #2438]](http://noticiasdelaciencia.com/upload/img/periodico/img_2438.jpg)
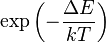 , donde
, donde